Вторичные метаболиты растений. Фенольные соединения и минорные группы.
Автор: Вишневская А.И.
Фенольные соедиинения.
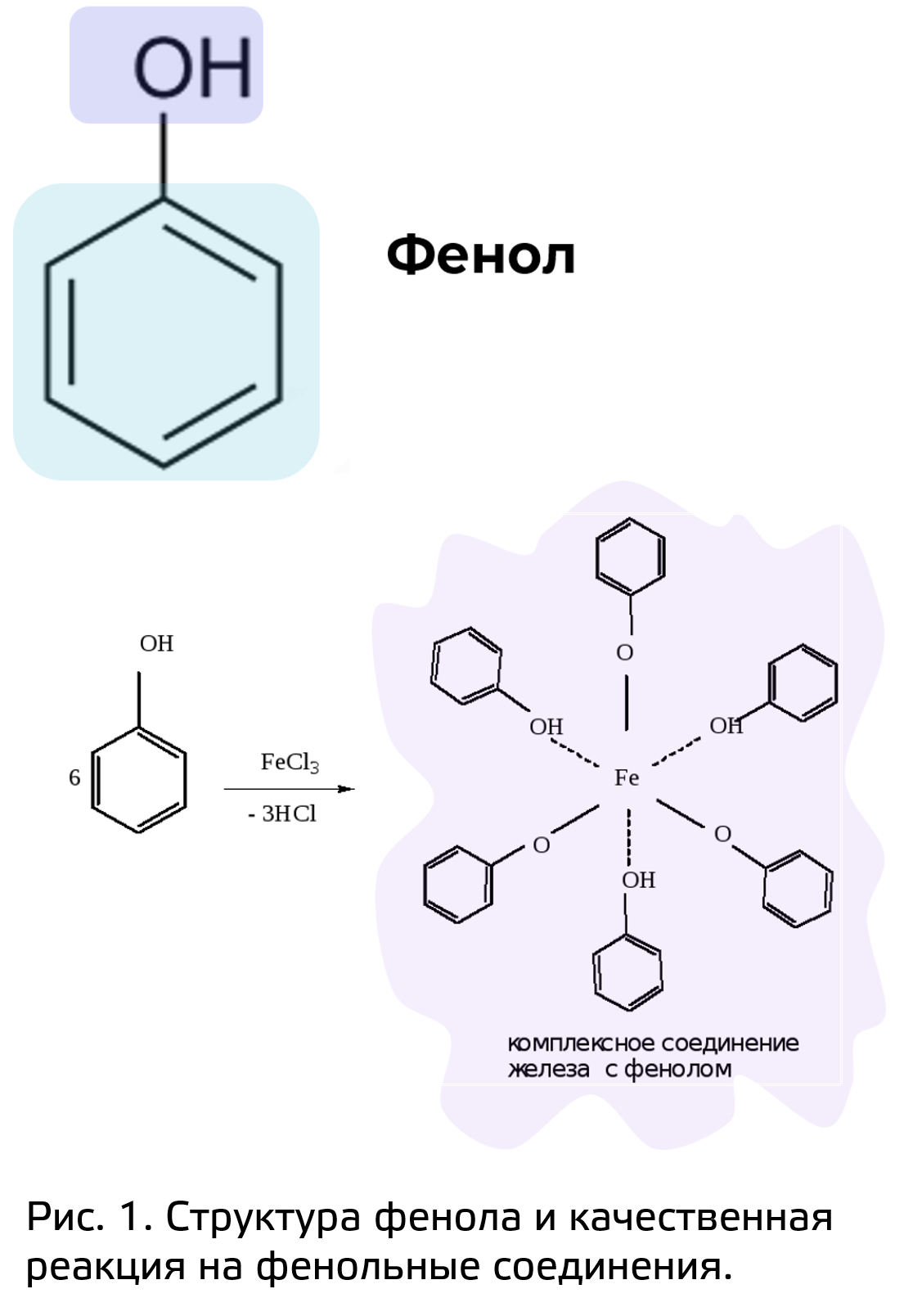
Фенольные соединения имеют своем составе ароматическое кольцо с одной или несколькими гидроксильными группами (рис. 1). Одной из качественных реакций на фенолы является реакция с FeCl3. В результате этой реакции образуется окрашенное соединение фиолетового цвета.
В основе химической классификации (рис. 2) может лежать два параметра:
- Количество бензольных колец;
- Количество атомов углерода вне цикла (экстрациклических).
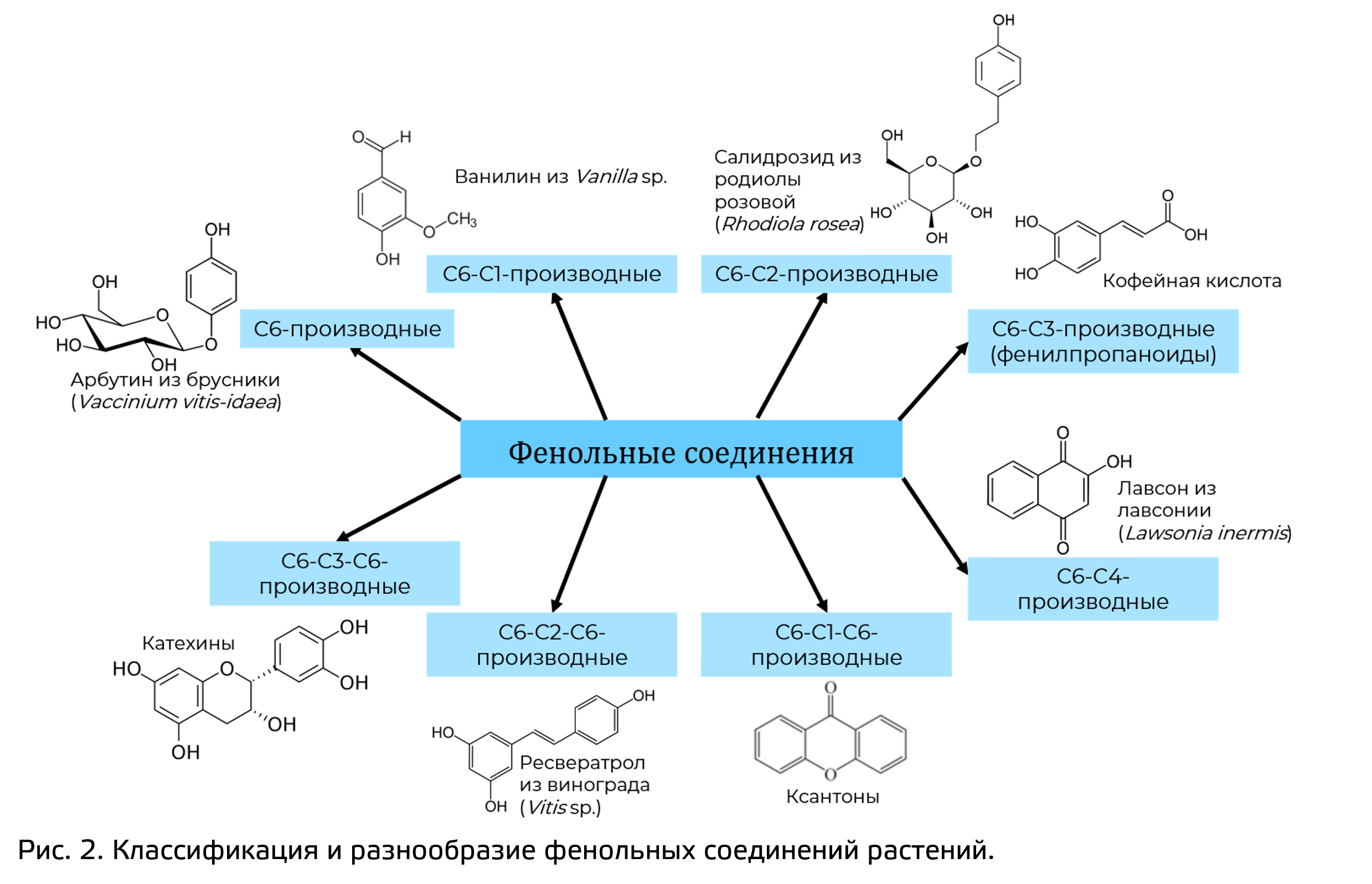
Однако такая классификация не дает никаких сведений о биосинтезе, а фенольные соединения, даже относящиеся к одной группе, могут иметь различные пути биосинтеза.
Биосинтез фенольных соединений.
У растений есть минимум два пути образования фенольных соединений: поликетидный и шикиматный. И снова, как и в случае с изопреноидами, один локализован в пластидах (это шикиматный путь – тот самый, который дает начало также ароматическим аминокислотам), а другой – в цитозоле (точнее на эндоплазматическом ретикулуме).
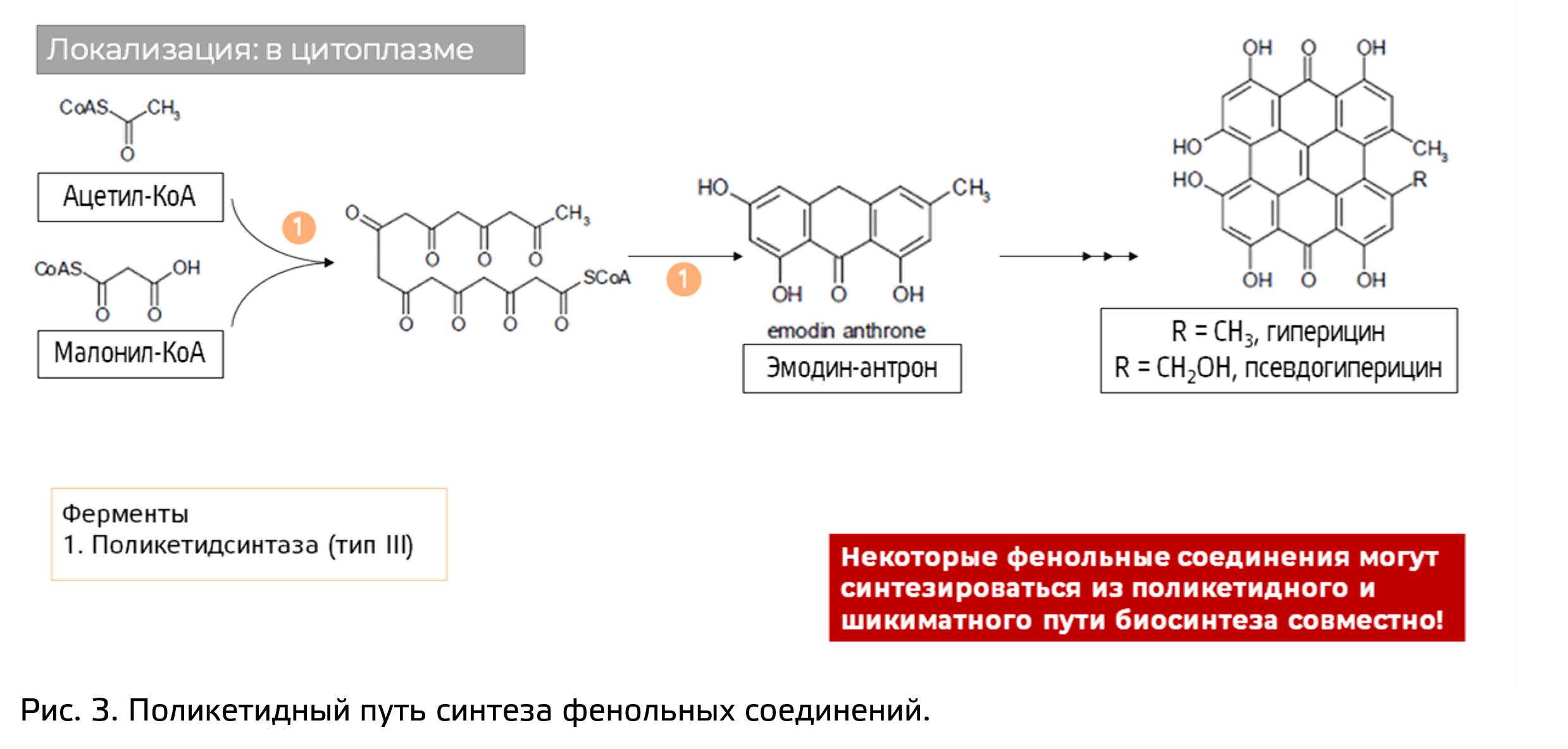
Поликетидный путь (рис. 3) начинается с конденсации нескольких остатков малонил-КоА. Здесь работает фермент поликетидсинтаза, локализованный на ЭПР.
Поликетидсинтаза присоединяют несколько остатков малоновой кислоты — образуется поликетид - промежуточный продукт (только в активном центре фермента), дальше он подвергается циклизации, дегидратируется с образованием ароматического второго кольца, которое затем гидроксилируется.
Шикиматный путь биосинтеза связан с обменов ароматический аминокислот и локализован в пластидах (рис. 4). Он начинается с ФЕП и эритрозо-4-фосфат (вспомните, откуда в растениях эти вещества), через последовательные стадии они преобразуются в шикимат, который далее направляется на синтез ароматических АК. Здесь правда может произойти разветвление. Дело в том, что некоторые С6-С1 соединения (например, галловая кислота) образуются из интермедиата этого пути биосинтеза - дегидрошикимовой кислоты. В ином случае шикимат преобразуется в хоризмовую кислоту, которая является непосредственным предшественником всех ароматических аминокислот. Часть харизмата идет на синтез тирозина и фенилаланина, другая часть хоризмата идет через стадию антраниловой кислоты. Из антраниловой кислоты синтезируется триптофан (как вы помните, и триптофан, и антраниловая кислота – предшественники некоторых алкалоидов). Синтез флавоноидов связан с обменом фенилаланина. Ключевая стадия синтеза фенольных стадий — фенилаланинаммиаклиаза — дезаминрование фенилаланина, с образованием двойной связи в боковой цепи. Тут, правда, стоит сказать, что именно эта реакция идет уже в цитозоле, то есть после того, как продукт шикиматного пути биосинтеза – фенилаланин выйдет из пластиды. В результате этой реакции образуется коричная кислота. Далее она может либо давать начало остальным фенилпропаноидам (С6-С3) соединениям, либо терять атомы углерода, приводя к образованию С6-С2 соединений, либо давать начало С6-С2-С6 и С6-С3-С6, таких как стильбены и у флавоноиды. Причём интересно, что у таких соединений как правило одно бензольное кольцо происходит из фенилаланина, а второе образуется поликетидными путем.
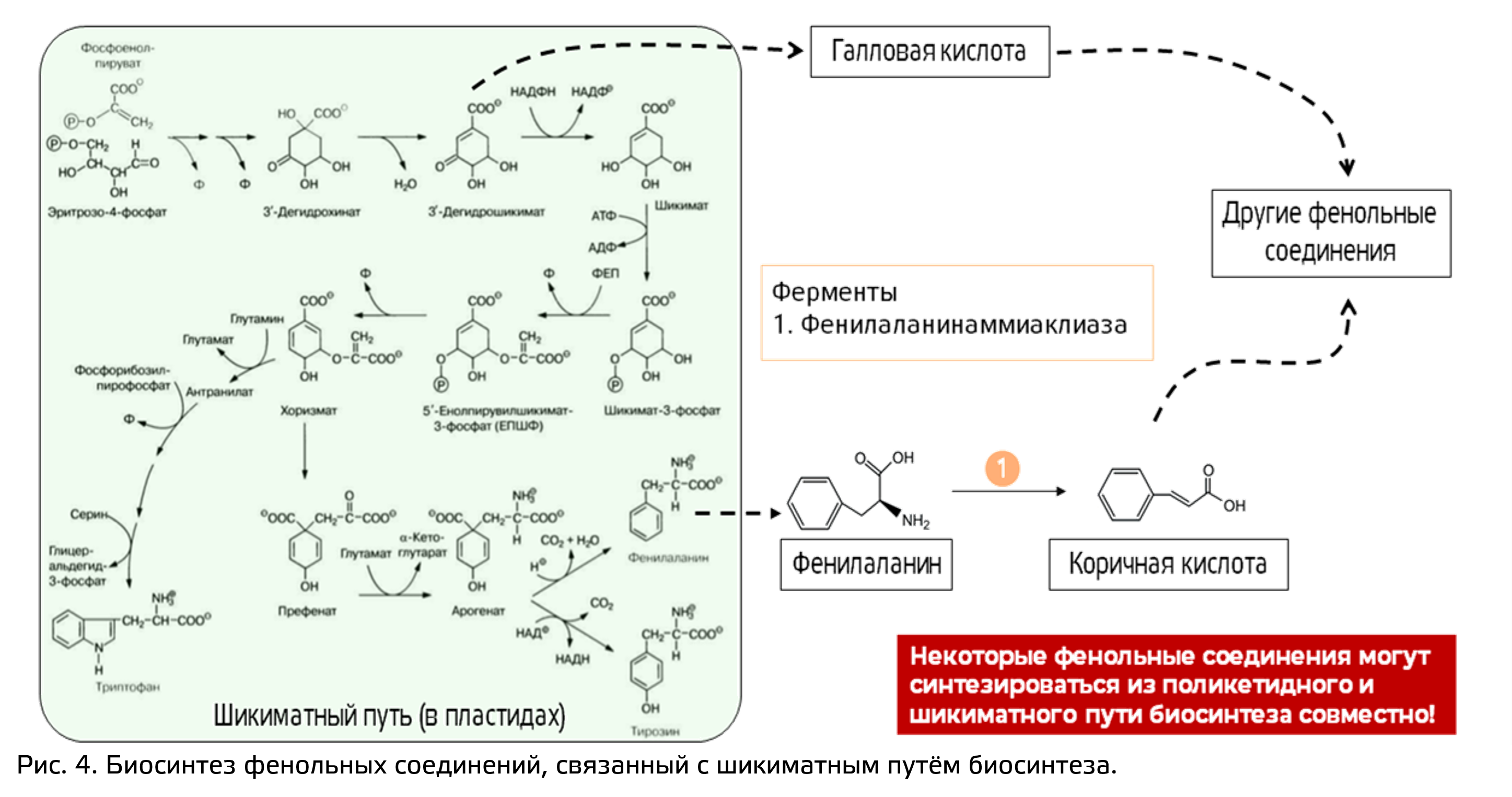
Из-за таких необычных, пересекающихся между собой путей биосинтеза фенольных соединений, классифицировать их по биосинтезу практически невозможно, так что классификация построена на основе их структуры.
Разнообразие фенольных соединений.
К группе С6-С1-производных относится очень важное соединение – галловая кислота. Галловая кислота дает начало целому спектру других вторичных метаболитов. Чаще всего она в свободном виде не накапливается, а вступает в образование сложных молекул. Например, присутствует в растении в виде конъюгатов с глюкозой.
Такие коньюгаты галловой кислоты с глюкозой также носят название гидролизуемых танинов, или дубильных веществ. Названа эта кислота так в честь патологических наростов, похожие на опухоли, галлы (рис. 5).

В них часто накапливаются вещества с выраженным вяжущим действием. Конечно, гидролизуемые танины (рис. 6) встречаются не только в дубе, но и в других растениях. Например, их много в соплодиях ольхи и корневищах бадана.
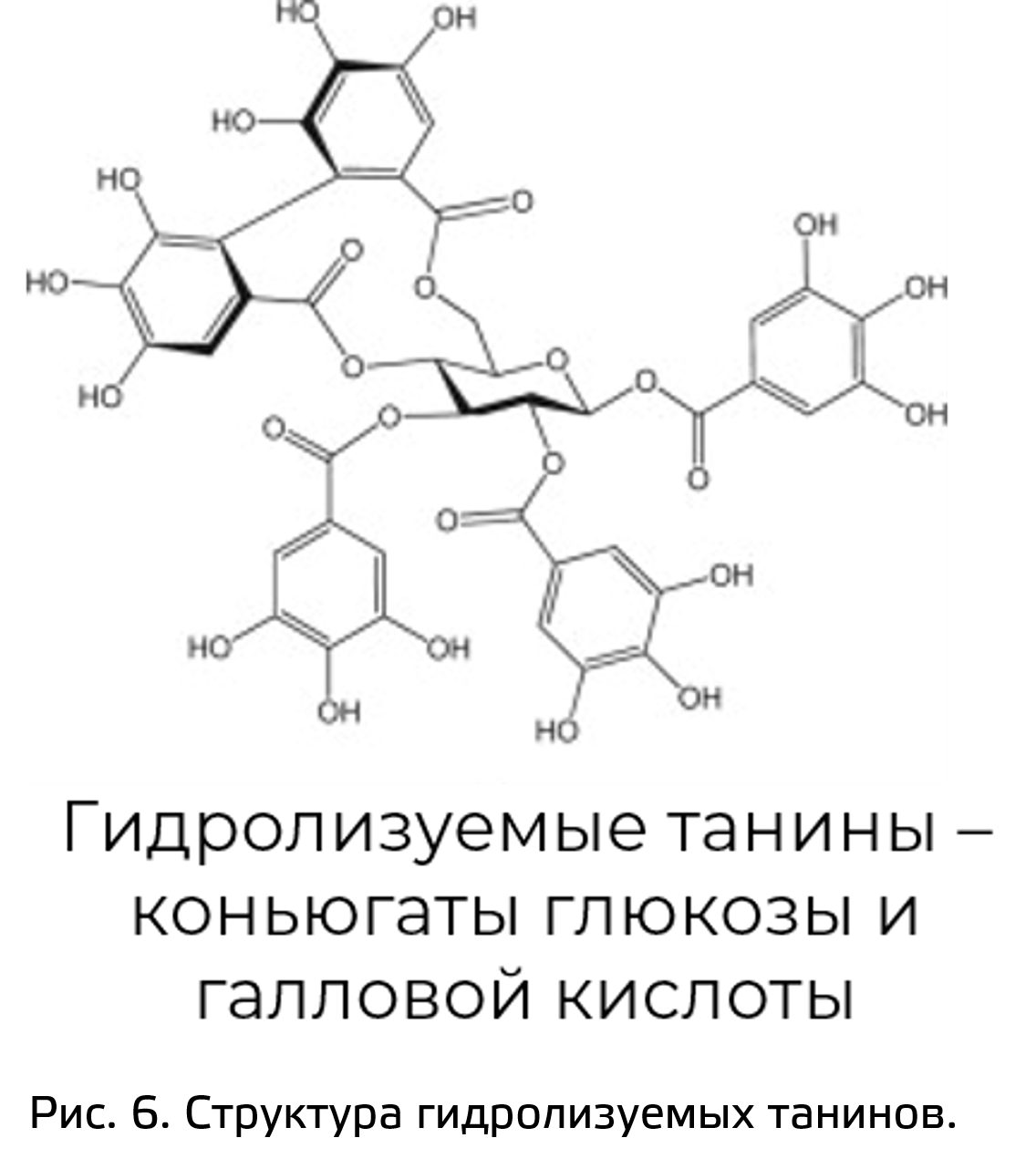
В молекулах танинов много гидроксильных групп, поэтому они могут взаимодействовать с биополимерами: при взаимодействии с белками, они денатурируют, а дубильные вещества таким образом они выполняют защитную роль в растении. С другой стороны, танины имеют хозяйственное значение для человека: раньше их использовали для выделки кожи. Из-за способности танинов денатурировать белки, они при воздействии на кожу приводят к поперечному сшиванию белков в ней — кожа становится долговечной и не гниет. Танины иногда используются и в медицине, например, при обработке ран, чтобы разрушать патогенные белки в ране.
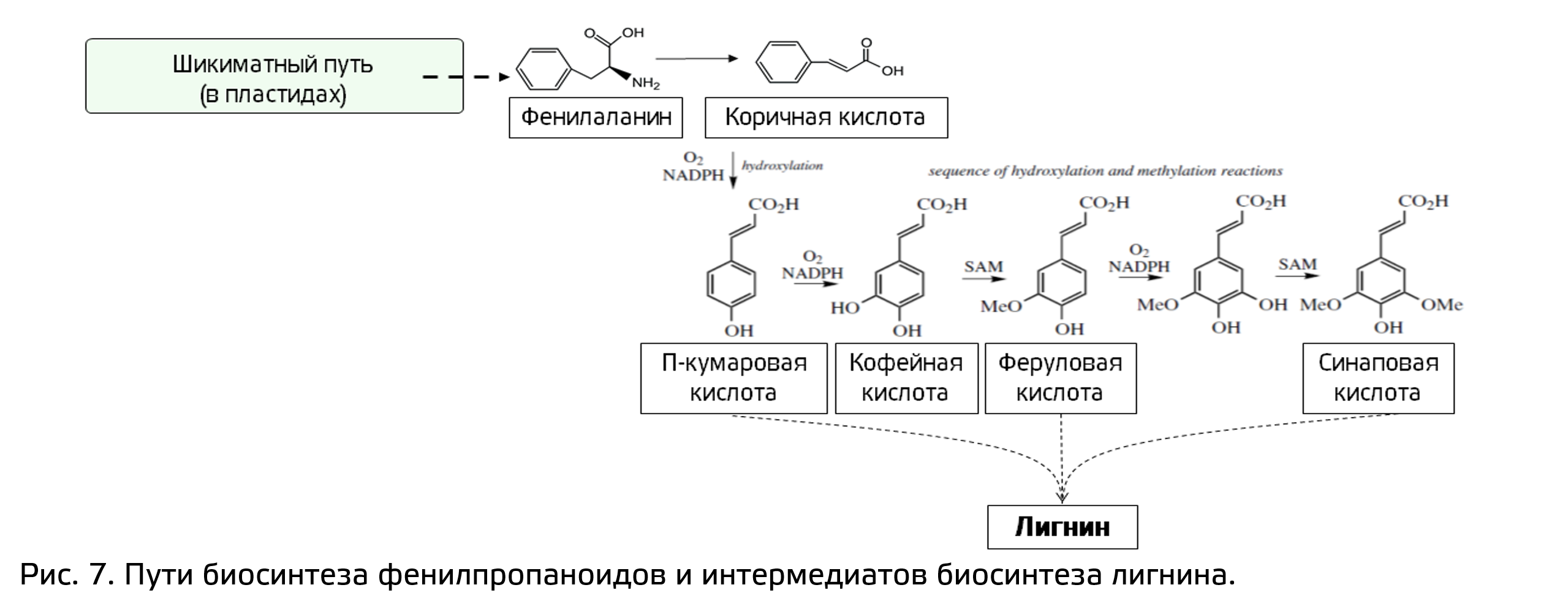
Одна из наиболее распространенных групп фенольных соединений – это фенилпропаноиды С6-С3 соединения. И это неспроста: именно они получаются при работе фенилаланинамиаклиазы из фенилаланина (рис. 7). А если быть точнее, получается гидроксикоричная кислота, из которой затем синтезируются как вторичные метаболиты, так и первичные. К примеру, кумаровый, конифероловый и синаповый спирты входят в состав лигнина: вещества, откладывающегося во вторичной клеточной стенке некоторых тканей растений (например, ксилемы и склеренхимы). Очевидно, очень трудно назвать лигнин вторичным метаболитом.
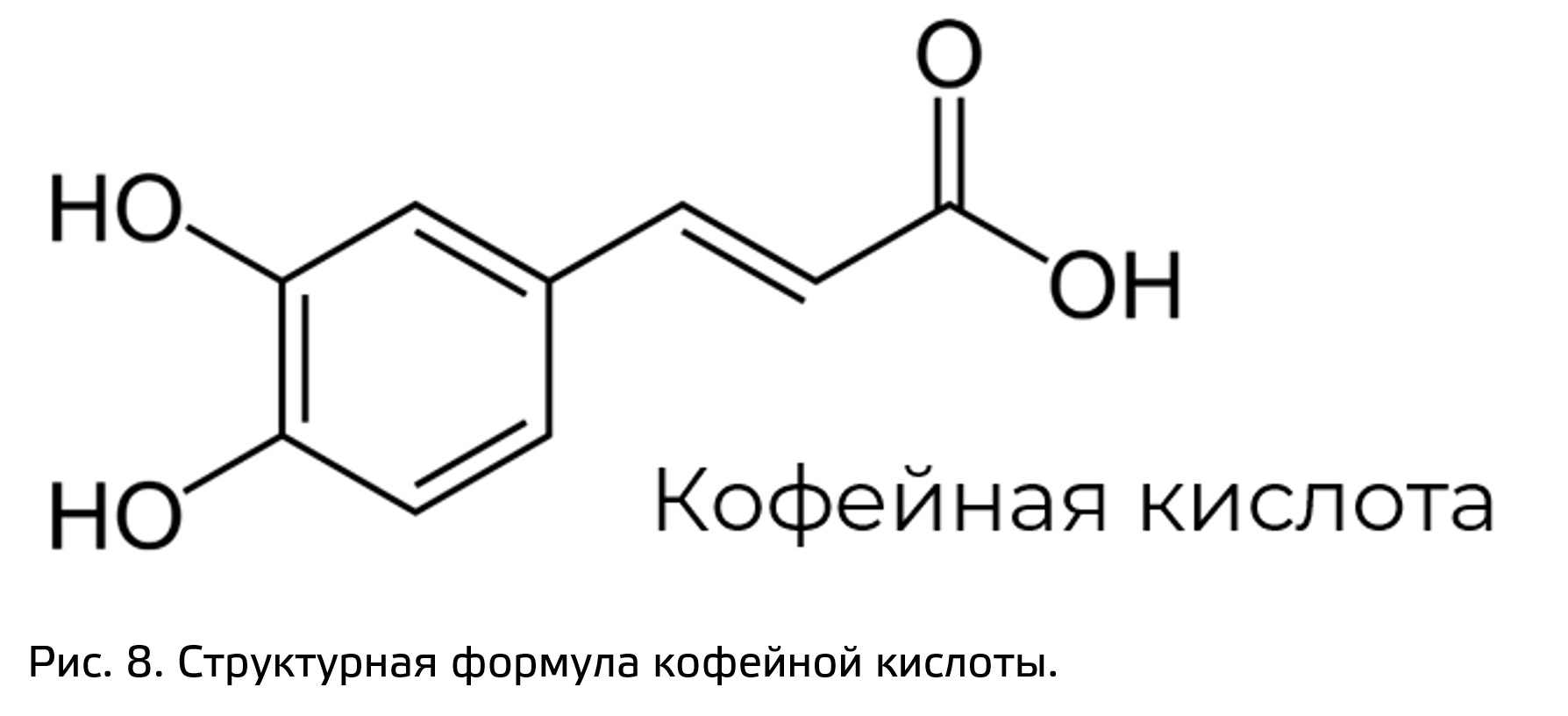
Одним из примеров фенилпропаноидов может служить кофейная кислота (рис. 8). Она может образовывать коньюгаты с самыми разными веществами, например с хинной кислотой. В такой коньюгированной форме кофейная кислота также называется хлорогеновой кислотой. Именно она придает тот горьковатый вкус кофе.
Если у кумаровой кислоты гидроксильная группа находиться в орто-положении, то карбоксильная группа может вступить с ней в реакцию с образованием соединений, объединенных под названием кумарины. Их вы тоже наверняка знаете, если хоть раз косили траву. Запах скошенной травы и есть в основном запах кумаринов. Предполагается, что в клетках растений ортокумаровая кислота накапливается в виде гликозидов в вакуоли. При нарушении целостности клетки ортокумарин гидролизуется и образуется летучий кумарин (рис. 9) с характерным запахом скошенной травы (это один из предположительных механизмов).
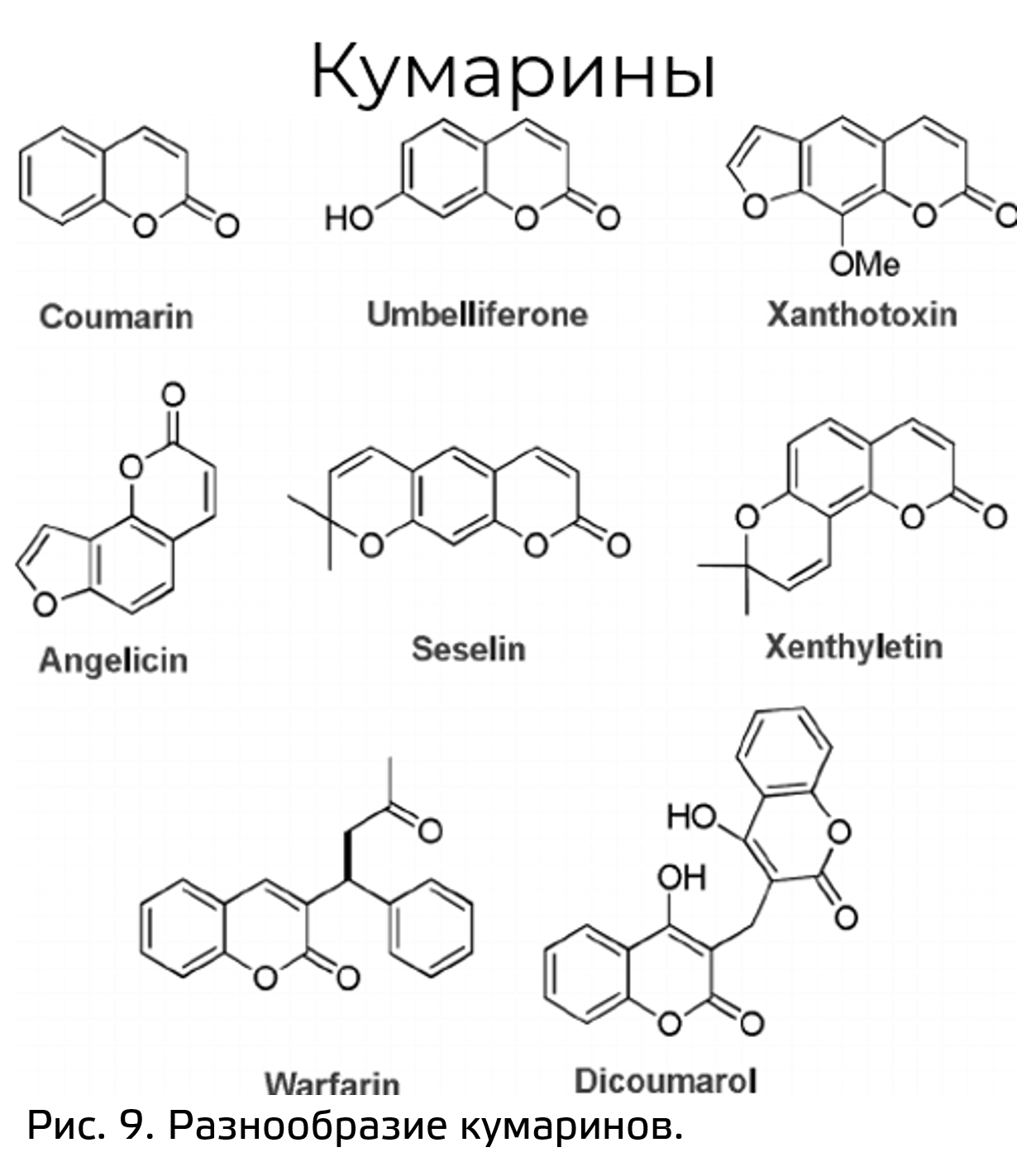
Кумарины могут димеризоваться с образованием дикумарола, который присутствует в сене, в траве донника. Это соединение снижает свертываемость крови, и В начале XX века из некоторых штатов на севере США и из нескольких провинций Канады поступили сообщения о случаях ранее не выявленного заболевания коров. По непонятным причинам у них возникали внутренние кровотечения, которые в конце концов приводили к летальным исходам. Причина крылась как раз в образовании дикумарола у донника.
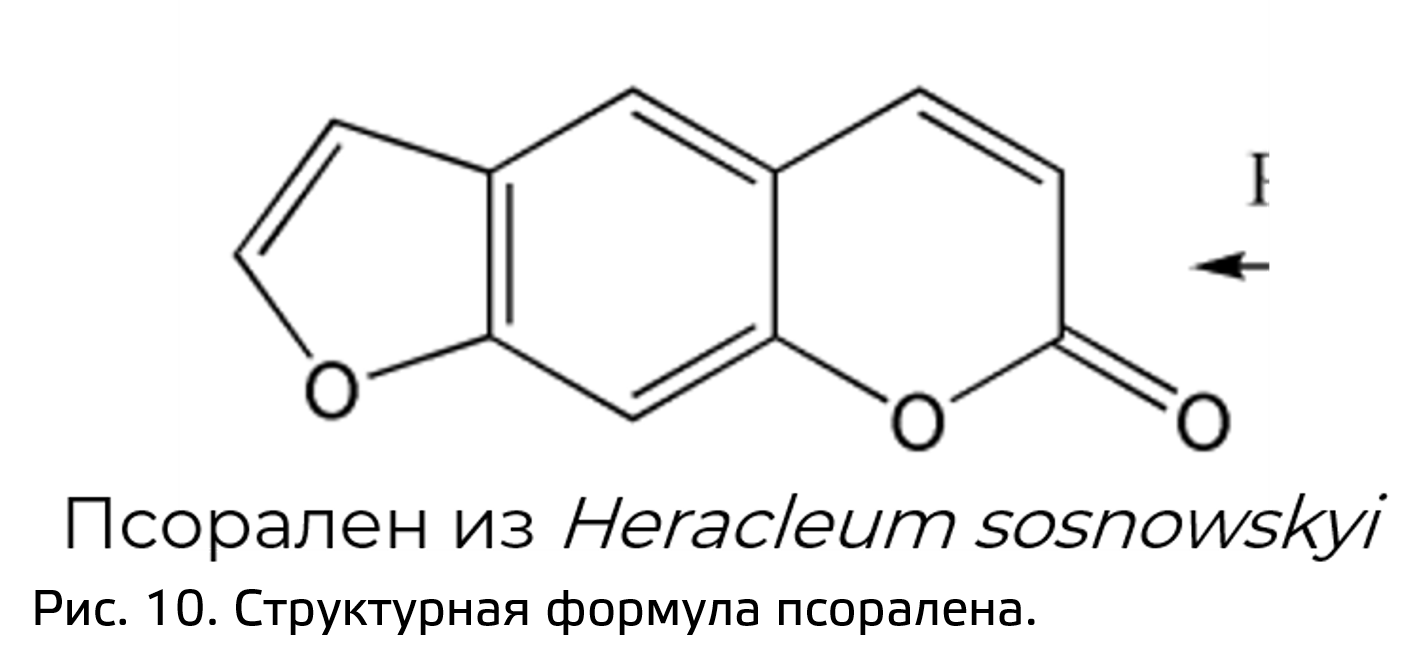
Для кумаринов характерны реакции принилирования, то есть присоединения изопреноидного остатка. Подобное принилирование приводит к образованию дополнительного кольца и такие соединения носят названия фуранокумарины. Одним из примеров фуранокумаринов может служить псорален (рис. 10). Именно он отвечает за возникновение ожога при контакте с борщевиком (Heracleum sosnowskyi). Однако есть способ избежать ожог. Дело в том, что фуранокумарины обладают фотосенсабилизацией, то есть активны только на свету. Если вы дотронулись до борщевика, как можно скорее закройте это место от света.
Очень важной и разнообразной группой фенольных соединений является группа С6-С3-С6 производных. Вещества, входящие в состав этой группы, также называют флавоноидами. Все это разнообразие нужно классифицировать и это делают по структуре срединной цепочки. Выделяют группы:
- Халконы
Полностью разомкнутая цепочка между двумя кольцами.
- Ауроны
Внутреняя цепочка формирует пятичелнное кольцо.
- Истинные флавоноиды
Имеют шестичленное пирановое кольцо.
Истинные флавоноиды делятся в свою очередь на еще ряд групп в зависимости от тех или иных функциональных групп (рис. 11).
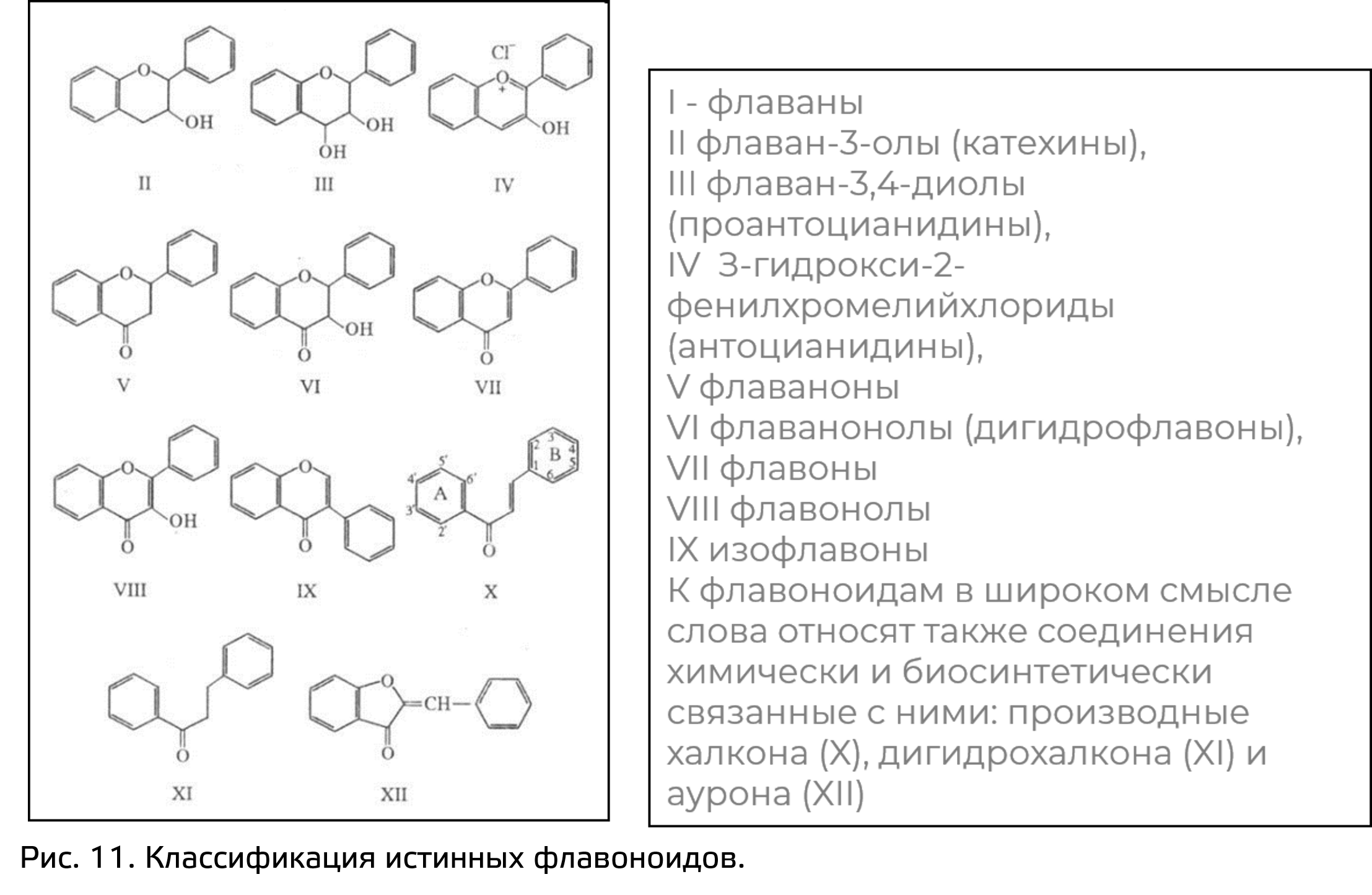
В этой статье мы разберем лишь некоторые из истинных флавоноидов.
К истинным флавоноидам относятся, например, катехины. Они накапливаются в растениях в свободном виде и очень распространены. Когда вы завариваете чай, катехины выходят в раствор и окрашивают чай в привычный вам цвет. Темная окраска чая связана с тем что катехины при ферментации окисляются, хотя сами по себе они бесцветны. Катехины часто обладают горьковато-вяжущим вкусом, хорошо растворимы в воде и спирте.
Катехины также являются негидролизуемыми танинами (рис. 12). Напомним, что гидролизуемые танины были представлены коньюгатами галловой кислоты.
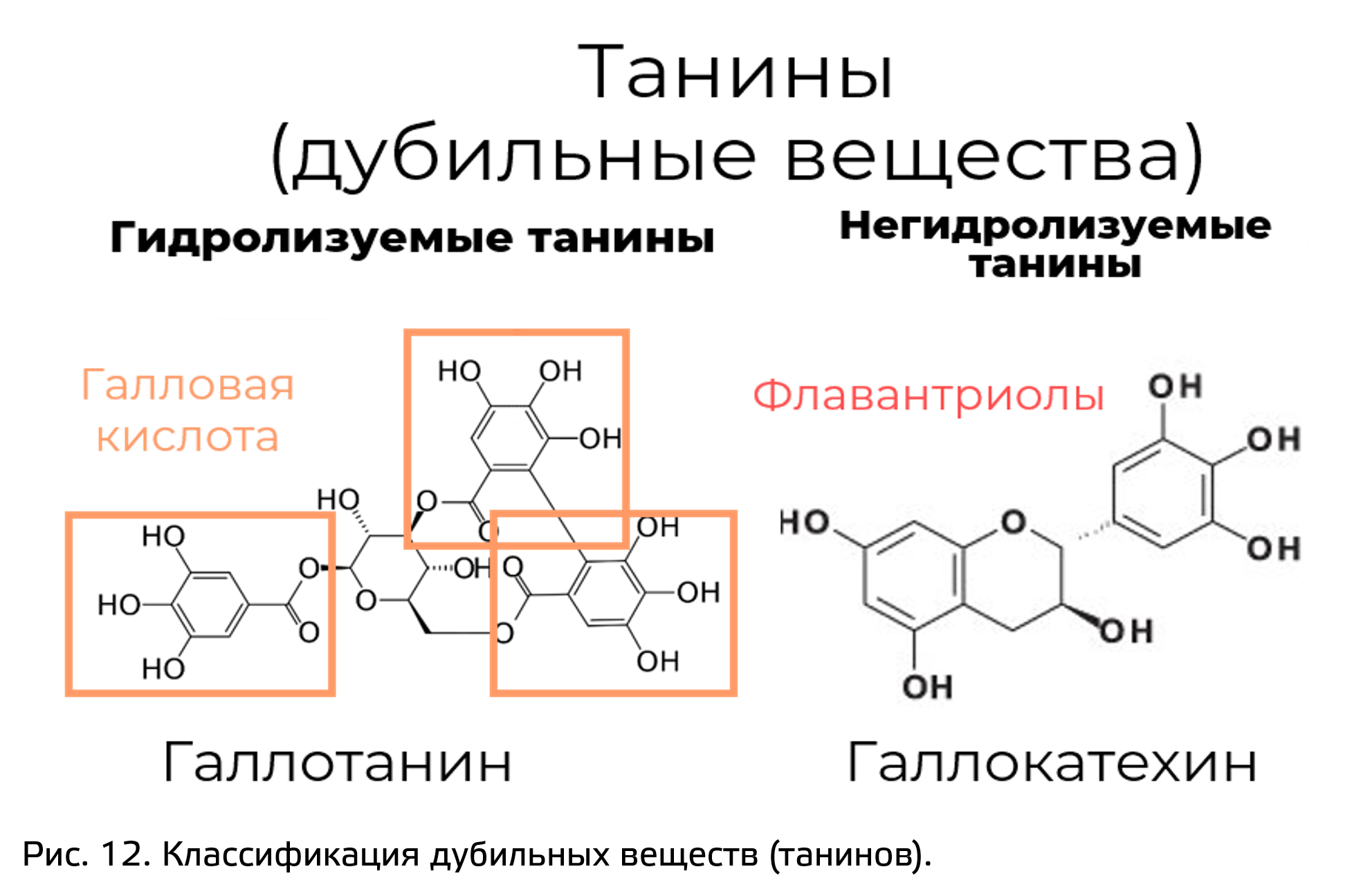
К С6-С3-С6 производным также относятся очень красивые вещества, придающие растениям самые необычные краски. Это группа антоцианы.
Важно сразу отметить, что то, что мы зовем антоцианами – не целиком флавоноид, а его соединение с глюкозой. Часть без глюкозы (агликон) зовётся антоцианидин (рис. 13).
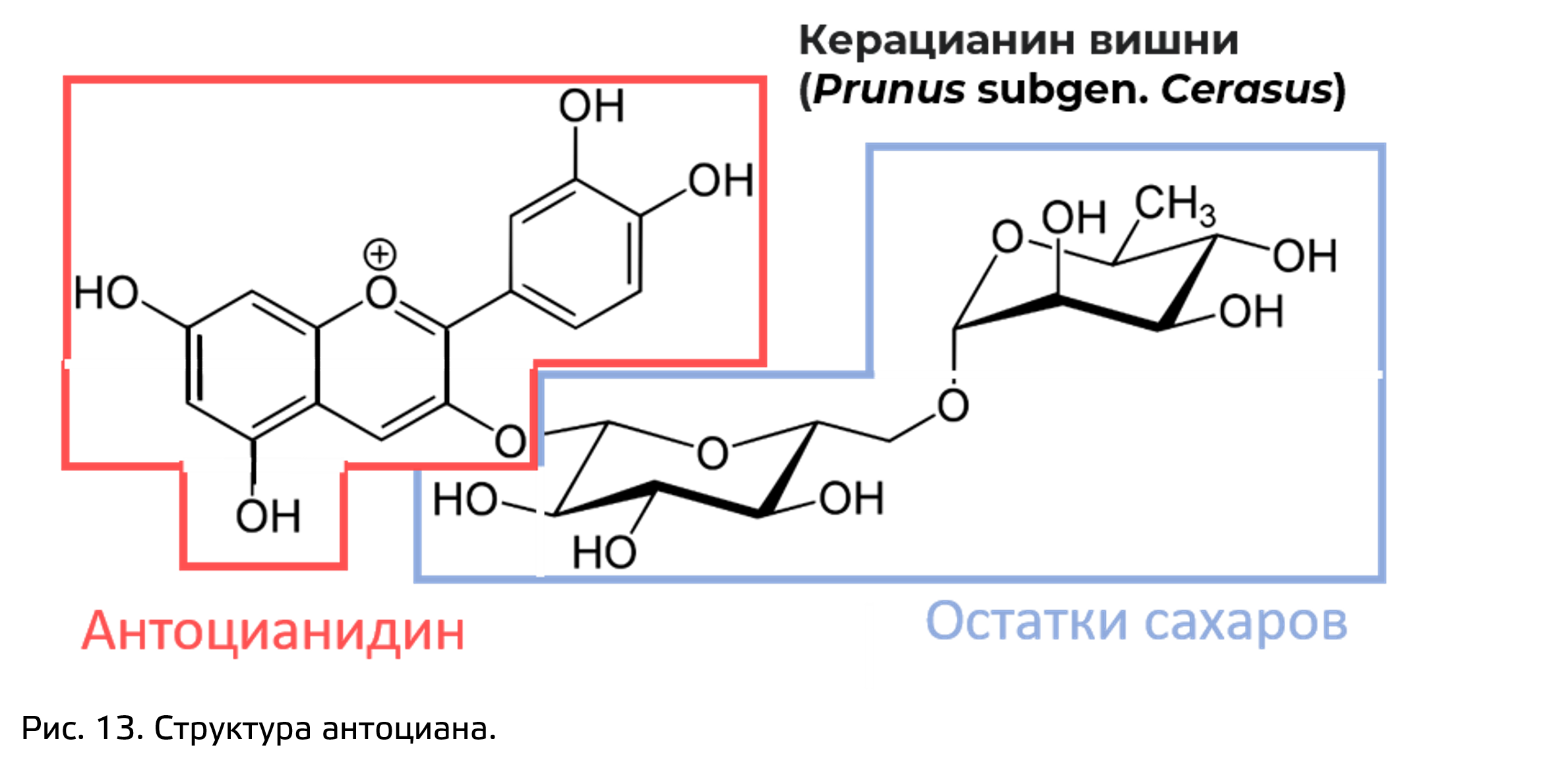
Антоцианы определяют многих частей растения и важны для привлечения опылителей. пигментное соединение с выраженной окраской. Эта окраска зависит от очень многих факторов. Например, от pH. Кроме того окраска зависит от структуры агликона, от копигментации, и от характера ацилирования. Копигментация заключается в том, что в зависимости от того какой ионный состав вокруг антоциана, спектр поглощения пигмента может сильно различаться. На самом деле агликонов антоцианов известно на так много, так что разнообразие антоцианидинов не очень большое, но именно разнообразие других факторов, влияющих на окраску, дает растениям возможность иметь столь разные окраски химически практически одинаковыми веществами. Важно отметить, что антоцианы помимо красящей функции также считаются важным копонентом защиты от активных форм кислорода. Не зря, например, при тех или иных нарушениях фотосинтетического аппарата или при каких-то абиотических стрессах листья приобретают красноватую окраску именно благодаря подобным соединениям.
Минорные группы.
Единого пути биосинтеза у всех минорных групп нет. Многие классы минорных вторичных метаболитов связаны с обменом аминокислот, другие с обменом жирных кислот или поликетидным синтезом.
К продуктам обмена аминокислот можно отнести:
- Небелковые аминокислоты (минорный класс, широко распространенный среди растений, играет важную биохимическую и защитную роль).
- Растительные амины (разнообразные амины, играющие физиологическую роль и в нашем организме)
- Цианогенные гликозиды (у нескольких сотен различных семейств и видов),
- Гликозиды горчичных масел (гликозинолаты, серосодержащие, меньше распространены, характерны для Крестоцветных).
- Беталаины (содержат в своем составе индольное ядро, могут быть в какой-то степени отнесены к алкалоидам, выполняют функцию пигментов-заместителей антоцианов).
Продукты обмена липидов:
- Необычные жирные кислоты
- Ацетиленовые производные содержат уникальные ацетиленовые группы, часто именуются полиацетиленами при том, что ацетиленовая связь в природе встречается редко. Грибы тоже синтезируют похожие соединения.
Политиофены, тиофеновое четырехчленое гетероциклическое ядро с серой, у растений их синтез начинается с формирования полиацетиленового производного.
Производные поликетидного синтеза: ацетогенины.
- Неклассические аминокислоты
Неклассические аминокислоты (рис. 14) часто связаны с образованием D-изомеров классических аминокислот. Напомним, что в белки входят только L-изомеры аминокислот. Кроме того, для группы непротеиногенных аминокислот очень часто характерны модификации: гидроксилирование, метилирование, ацилирование.
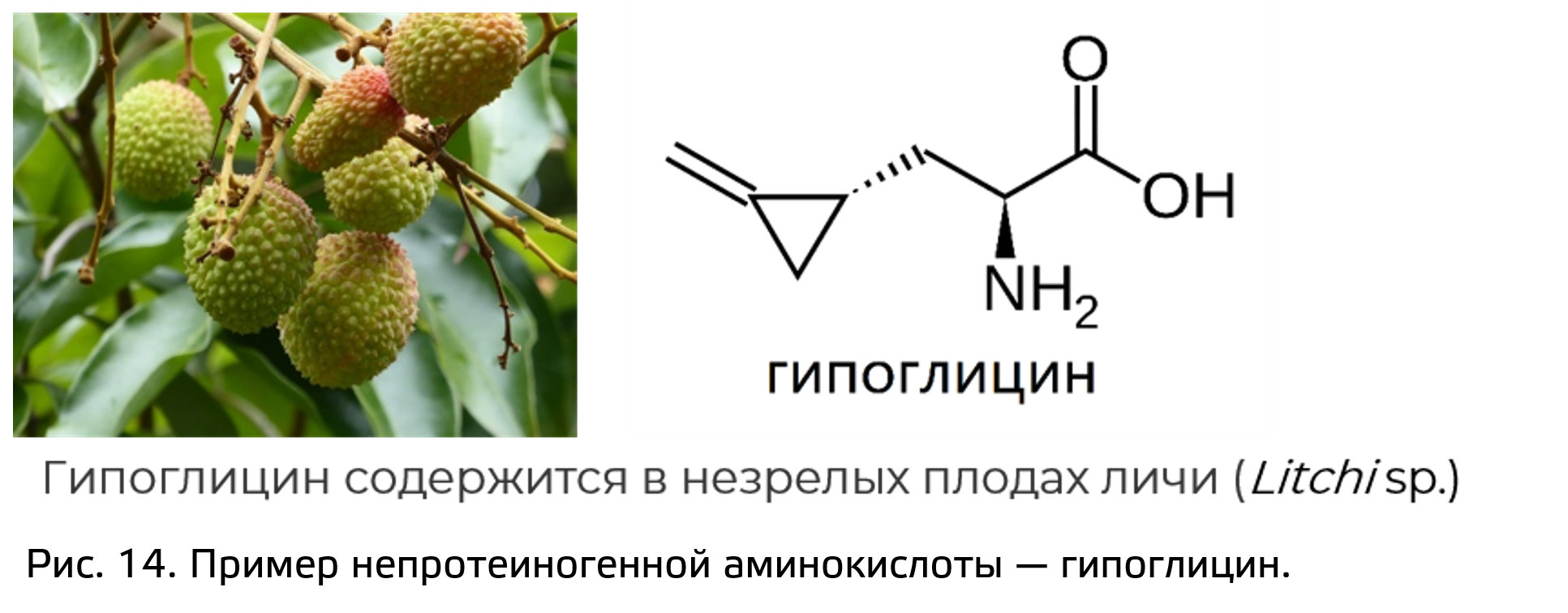
Типичный пример – цистеин, у которого атом серы заменен на селен, силеноцистеин. НО называть селенцистеин непртеиногенной аминокислотой не совсем корректоно, так как он входит в состав активных центров некоторых ферментов (например, он есть в активном центре глутатионпероксидазы). В то же время большое количество свободного селеносцистеина – это яд для животных, польку по ошибке такие аминокислоты могут встраиваться на место цистеинов, что в итоге приводит к синтезу нефункциональных белков.
- Биогенные амины.
В основном биогенные амины представляют собой либо продукты метаболизма аминокислот, либо продукты метаболизма (переаминирования) альдегидов. В то же время, эти соединения по структуре можно также отнести к протоалкалоидам. Выделение их в отдельную группу подчеркивает особенность по распространенности. И если у животных такие биогенные амины выполняют первичные функции, связанные с функционированием нервной системы (серотонин) или в воспалительных процессах (гистамин (рис. 15)), то у растений это в первую очередь защитные вещества.

- Бетаины
Четвертичные соли аминов выделяют в отдельную группу – бетаины. Не путайте эти соединения с беталаинами!
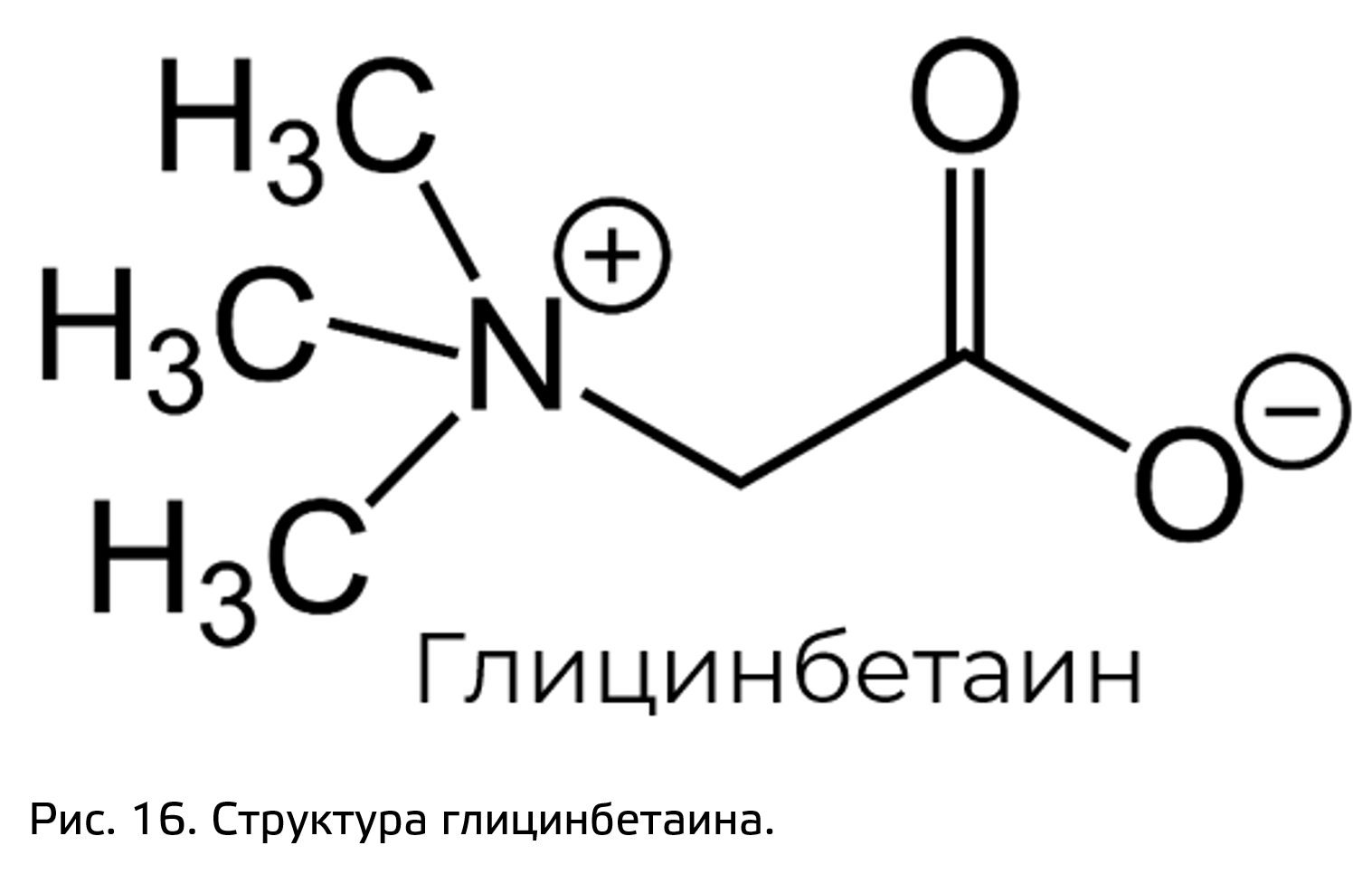
Особенно широко распространено такое вещество, как глицинбетаин. Интересно, что некоторые вторичные метаболиты способны защищать растения не только от биотического стресса, но и от абиотического. Глицинбетаин (рис. 16) является признанным осмолитиком, т.е. веществом помогающим растению сохранить в себе воду.
- Цианогенные гликозиды
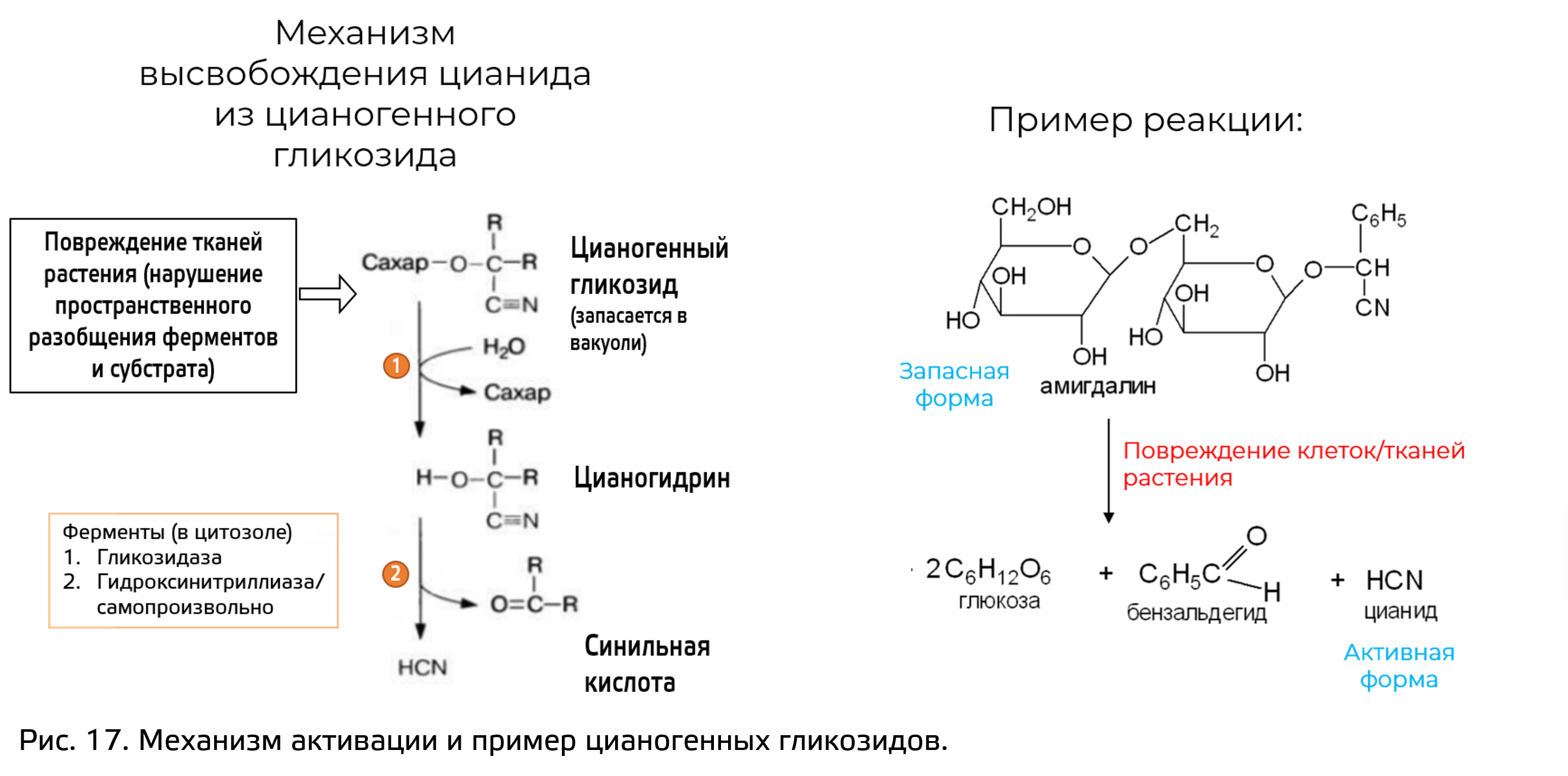
Уже по названию понятно, что они способны продуцировать цианид – ингибитор четвертого комплекса ЭТЦ митохондрий. В интактных растениях такие вещества накапливаются в вакуолях в виде гликозилированной формы. Активирующий фермент гликозидаза пространственно разобщена с субстратом (на уровне клетки или на уровне специализации тканей). Активация только ответ на стрессовые ситуации: например, при нарушении целостности растительных тканей или клеток неактивные предшественники встречаются с активирующим ферментом, образуется нестабильный агликон. Агликон либо самопроизвольно, либо под действием фермента нитрилазы разрушается, и выделяется синильная кислота (рис. 17). Напоминим, что такой механизмы защиты вторичными метаболитами дает нам возможность назвать их полуиндуцибельными вторичными метабольитами.
- Цианолипиды
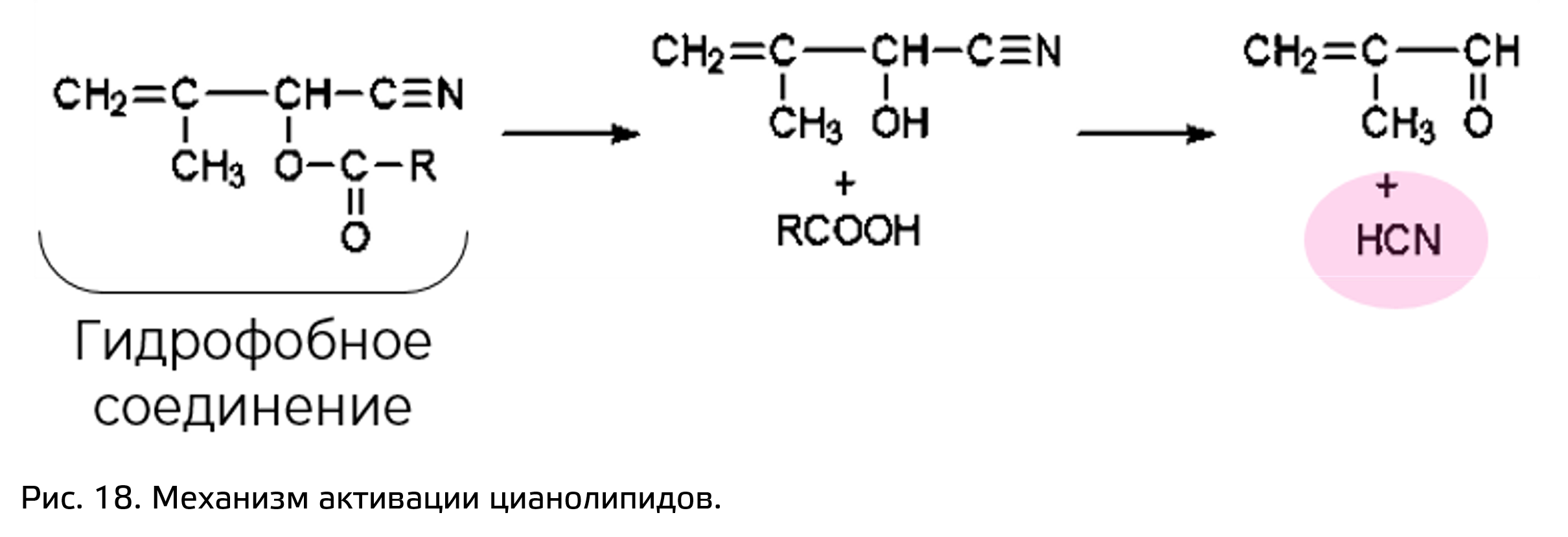
Есть и другие продуцирующие цианид соединения. Цианогенные гликозиды гидрофильны, поэтому накапливаются в вакуолях. Некоторые растения используют в качестве таких метаболитов гидрофобные цианогенные соединения – цианолипиды. При гидролизе образуются циангидрины, которые будут давать начало синильной кислоте (рис. 18). Но подобная стратегия не очень распространена.
Здесь гидроксильная группа стабилизирована не за счёт гликозилирования, а за счёт образования сложного эфира с жирной кислотой. Механизм работы аналогичен. Эстеразы гидролизуют сложный эфир с образованием нестабильного циангидрина с выделением жирных кислот (а не сахара). Дальше циангидрин расщепляется на цианид и альдегид.
- Глюкозинолаты
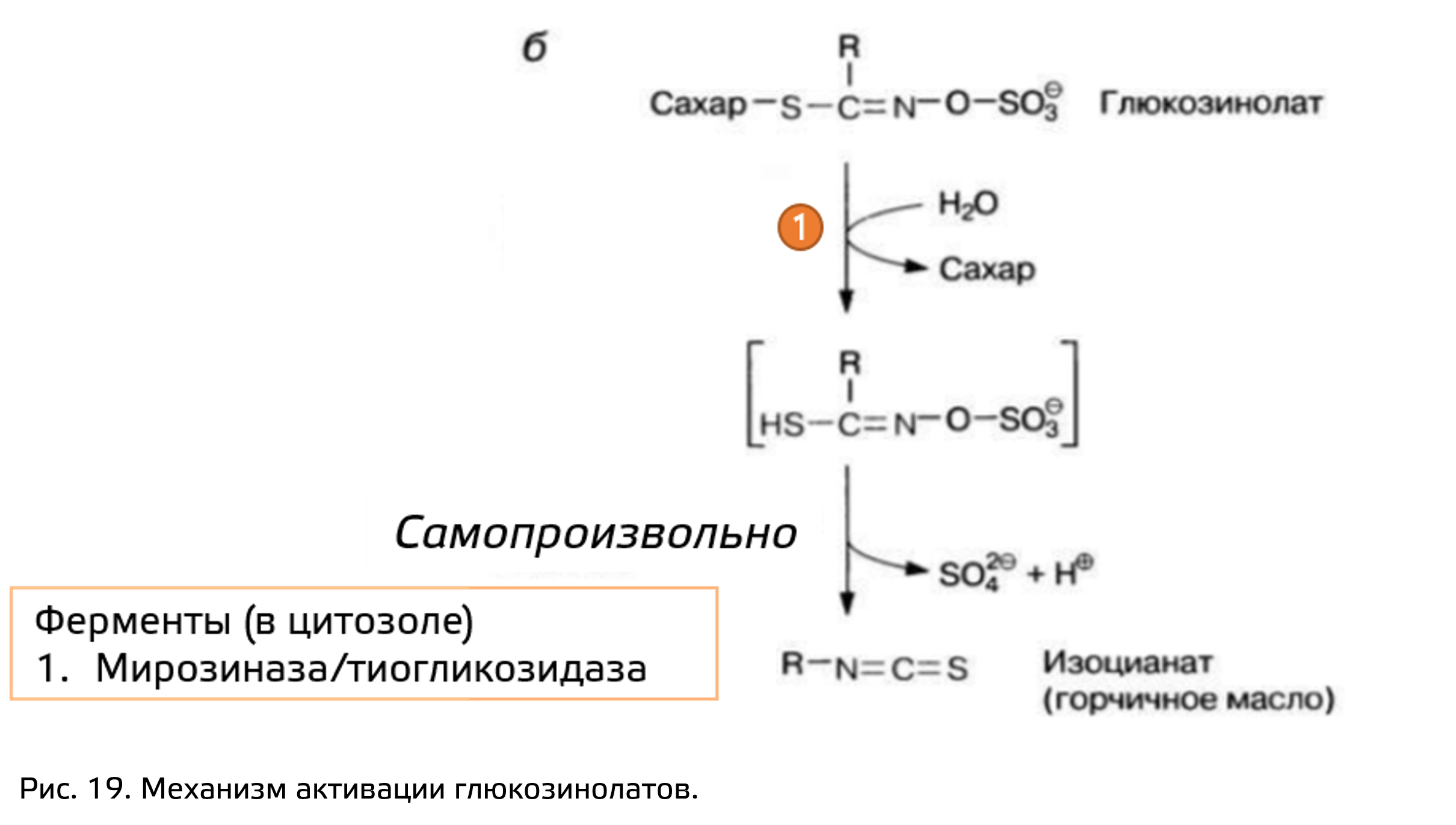
У семейства крестоцветные очень распространены серосодержащие соединения, способные продуцировать изоцианаты, – глюкозинолаты. Центром гликозилирования могу быть разные функциональные группы. Гликозилирование может происходить по гидроксильной группе, по азотной, по углероду, но может и по сере с образованием тиогликозидов.
Глюкозинолаты, или гликозиды горчичных масел, по своей структуре нестабильны. В результате гидролиза тиогликозидов образуется нестабильный агликон, который очень быстро перегруппировывается. Разрушение тиогликозидов осуществляется мирозиназой. Этот фермент пространственно разделён с самими глюкозинолатами (рис. 19). Глюкозинолаты накапливаются в вакуоли, а фермент – в цитоплазме. Таким образом, глюкозинолаты – еще один пример полуиндуцибельных вторичных метаболитов.
- Аллиины и аллицины
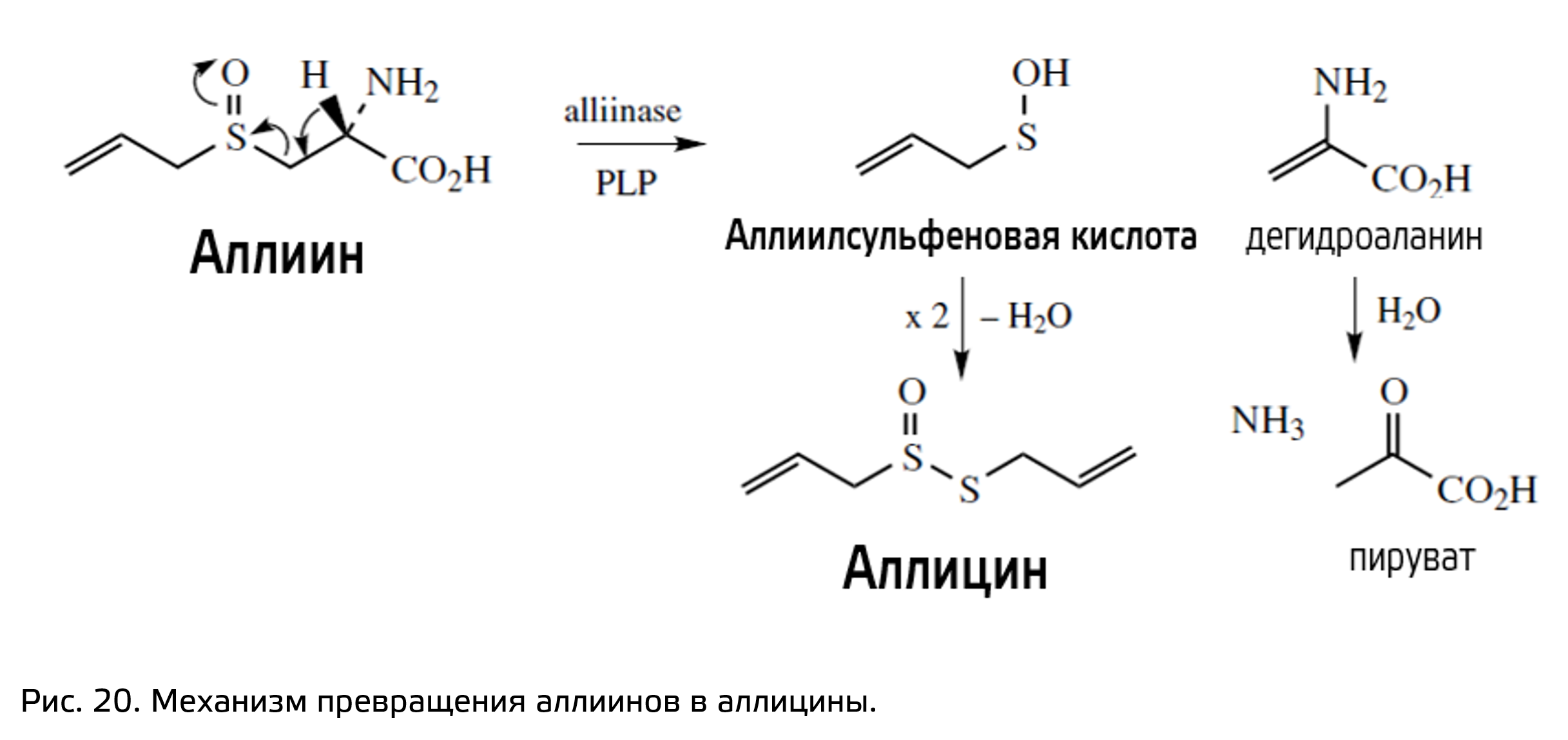
Аллиины являются продуктами преобразования цистеина и содержат в своём составе серу. К цистеину по сульфгидрильной группе происходит присоединение аллильной группы, после чего происходит окисление атома серы до сульфоксидного состояния. Аллиин это, по сути, тоже непротеиногенная аминокислота, но уникальность распространения и механизм действия позволяет выделить эти вещества в отдельную группу. Именно они обуславливают органолептические ощущения от лука и чеснока: аллиин расщепляется аллииназой на аллилсульфеновую кислоту (аллильная часть с атомом серы) и часть, которая потом самопроизвольно преобразуется в пируват. Аллиилсульфеновая кислота очень реакционноспособна, и два ее остатка димеризуется с образованием между ними S-S связи — получается димер аллицин (рис. 20). Именно он и придаёт луку слезоточивые свойства. И, как вы можете догадаться, в интактных растениях аллицины не присутствуют.
- Беталаины.
Беталаины представляют собой окрашенные азотсодержащие вещества. У растений, у которых есть беталаины, нет антоцианов, однако способность к синтезу флавоноидов есть. Они встречаются у растений порядка Гвоздичноцветные (Caryophyllales). Подобное ограниченное распределение беталаинов среди растений является синапоморфией для порядка Caryophyllales. Среди беталаинов есть красноокрашенные соединения – бетацианины, и жёлтоокрашенные – бетаксантины (рис. 21). Они отличаются не только по спектру поглощения, но и структурно: бетаксантины зачастую образуют коньюгаты с глюкозой, а бетаксантины – с остатками глюкозы или карбоновых кислот. Как и антоцианы, окраска беталаинов зависит от pH среды, однако если антоцианы могут обратимо изменять цвет при переходе из кислой среды в щелочную и обратно, то беталаины в сильно кислотной среде необратимо меняют свою окраску.